第二回です。前回に引き続き。
どこまで話していたかというと免疫システムにはそして獲得免疫と自然免疫がある。
そして獲得免疫をまず見ていくことにしていました。
獲得免疫の主人公の一つはリンパ球ですが、これはB細胞とT細胞に分かれていました。
そして、B細胞は抗体をつくって液性免疫を担い、T細胞は細胞を殺すことができて、細胞性免疫を担う。という話まで来ていました。
さてはて、ここまで分類しましたが、進めていきましょう。
T細胞はペプチドを認識する
T細胞は病原体をどうやって認識するのか?免疫の説明をするときにはいつでもわかりやすく話をうまく組み立てていくのは難しいのですが、まずはT細胞の認識の仕方、ここから攻めます。
さっと答えからいうと、病原体の持っているタンパク質 (protein) の一部である、ペプチド (peptide)、すなわちアミノ酸 (amino acid)の繋がった「鎖」を認識して、病原体をみつけます。
タンパク質というのはアミノ酸が鎖のようにながーくつながってできているんですね。アミノ酸は、全部で20種類が使われますが、それぞれが手をつなぐように結合していきます。
パーツであるアミノ酸一つ一つについては、ウイルスのものもヒトのものも同じ成分なので違いはありません。そこで何の差をみるかというと、「鎖の配列」を見分けるんですね 。
繰り返しますが、アミノ酸は20種つかわれます。そうすると、例えばペプチド鎖が10個であれば、20の10乗の組み合わせが作れることになります。すごい数です。
そうすると、たとえ10個ぐらいのアミノ酸がつながった短い鎖であっても、病原体に特有で、それでいてかつ、ヒトには存在していない、そういう配列の鎖が作られうるんですね。
細かい機構は後回しにして、こういったペプチド鎖を認識する仕組みをT細胞はもっている、とまずは考えておきます。
抗体も認識するのはペプチド
さて、突然また一度話がとびますが、実はB細胞の作る“ミサイル”である抗体もペプチド鎖を認識します。
病原体のペプチド鎖を認識するんですが、時にそれは大きなタンパク質そのものの一部だったりします。
つまりB細胞の作る抗体もT細胞もペプチド鎖を認識する
まとめるとB細胞のつくる抗体も、T細胞も、病原体のペプチド鎖の配列を読んで“敵”を認識するわけです。
T細胞やB細胞のつくる抗体は配列を認識する…すなわち配列を読む(?) どういうこと?
となりますが、仕組みは簡単です。ある一つの抗体はある一つの配列としかくっつかないのです。あるひとつのT細胞は、ある一つのペプチド鎖でしか刺激されないのです。
これが免疫学の大発展に繋がったキーポイントです。
もう一度噛み砕くと、B細胞は1種類のペプチドを認識する抗体しかつくりません。1つの細胞が1種類だけをつくります。
T細胞も同じく、1つの細胞は1種類のペプチド鎖を認識します。
無数の敵に対応するには
では、100万種類の病原体を認識するのにはどうすればよいか… 。
答えはシンプルに、100万種類、B細胞とT細胞を作ればいいのです。
さてはて、ヒトの遺伝子は2万5千個もないのです…。その時点で100万種類の抗体や100万種類のT細胞は作れない気がしますね。
その当時の常識的にはそうでした。しかし、すごい発見があったわけです。
それが、遺伝子をコードするDNAの編集がリンパ球では起こり、遺伝子を書き換える仕組みが存在する、ということです。
遺伝子はヒトをはじめ一個体内ではどの細胞でも同じ情報、同じ配列、同じ状態で安定してる。そういう「常識」がぶち壊される仕組みがあったわけです。
VDJ 遺伝子再構成
細かいことは除きますが、まず抗体から見ていきます。
抗体は重鎖2個と軽鎖2個の4つのパーツが組み合わされてできていますが、重鎖そのものもいくつかのパーツのツギハギでできています。
実はB細胞は、発達する段階のあるところで、この重鎖にどのパーツをつかうかという組み合わせがランダムに選択され、DNAそのものが編集されます。
これが VDJ 遺伝子再構成といわれる、驚きのしくみです。
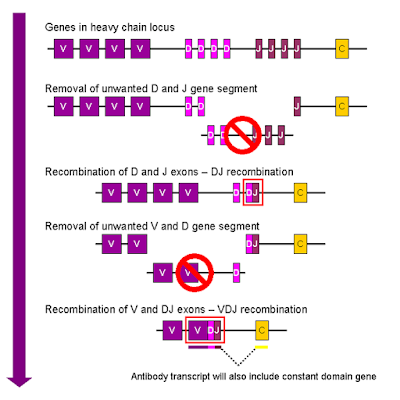
この図は重い鎖の部分をコードしているDNAの概念図です。
図の一番上は、今まで受け継いできたDNAです。Vという4つの箱、Dという4つの箱、Jという4つの箱が描かれています。
下に向かうにしたがって、これはB細胞のなかでDNAが組換えれる様子を表しています。
VやDなどの箱からランダムに1つずつをえらんで、一番下のようにつなげて組換えてしまう。こういうことが起こります。これを VDJ再構成 (V(D)J recombinationまたはsomatic recombination)といっています。
図では簡略化されていますが、実際にはたくさん“箱”があり、V部分が50の遺伝子断片、D部分30の遺伝子断片、J部分が6種類の遺伝子断片とすると、50×30×6 = 9000種類が作れることになります。実際には、抗体の重鎖部位は44個のV 、27個のD、6個のJがあります。
実は軽鎖にも同じような構成があり、いろいろと計算しますと約3000億種類の抗体をつくることができることになります。
この仕組みを見つけたのが利根川進先生で、これでノーベル賞を取っています。そのぐらいすごいことですね。
体細胞超変異
しかし、生物はまだまだもっといろいろなパターンの抗体を作る仕組みがあるんです。さらに凄いことがおこります。
抗体のV領域は抗体の最先端の部位で、ペプチドと直接くっつくところなのですが、ここの塩基配列がこれまたランダムに変えられてしまうのです。塩基配列というのはDNAの文字のことですね。
これを体細胞超変異 (somatic hypermutation; SHM)といいますが、これを起こす遺伝子がAID、そうあの本庶先生が見つけ、ノーベル賞をこれでとりたかったのだろうとさえ思われる、スーパー大発見だったのですね。
つまり抗体は、
さて、いちどまとめますと、抗体はB細胞がつくります。B細胞は発達段階で自分の抗体の遺伝子を組換え、超変異を起こします。
それらがそれぞれの細胞で起こるので、様々な種類の抗体をつくるB細胞が生まれてきます。ただし、1つのB細胞は1種類の抗体だけをつくると考えてください。
B細胞はわかった。T細胞は?
さてさて、T細胞、忘れてません。
T細胞も一つの細胞は1種類のペプチド鎖を認識するのでした。
ここで登場するのが分子なのですが、T細胞がペプチドを認識する、そのために使う分子が、T細胞の表面にくっついているT細胞受容体(TCR、T cell receptor) です。
TCR は複数の分子の塊からなっています。
このTCRも、抗体同様にパーツの組み合わせをランダムにすることと、超変異ではなく、TdTという分子がおこすのですが、先端部分のDNAの塩基配列を変更する仕組みで大量の種類が作られます。
理論的には上10の18乗ぐらいできます。
100万なんて超えましたね、軽く。
ここでもまた、T細胞一つは1種類のTCRをもつ、すなわち1種類のペプチドを認識することはかわりません。
ランダムに作りっぱなしか
さて、ここで一度くぎりますと、B細胞もT細胞も、自分の遺伝子をいじくっていろんなパターンの細胞を作ってしまうということが分かりました。
では、これら作られたすべての細胞が体に残り、働くのか、といえば、そうじゃないんです。ちゃんとセレクションするんですね。
細かい仕組みはまずは省きますが、自分の体由来のペプチドに強く反応してしまうT細胞は有害なので死にますし、ペプチドをうまく認識できない細胞も死にます。
これは、T細胞に関しては胸腺という心臓の上にある部分でおこります
この選択のはなしだけでも膨大な知識になるのがすごいのですが、今は取り敢えず、ペプチドを認識できて、かつ、自分由来のペプチドには反応しないT細胞だけが生き残っている、と考えてみます
実際にはB細胞はちょっと違いますが、いまは似たようなものと考えておきましょう。
さて、そうすると、身体の中には、自分は攻撃しないけど、“敵”のペプチド鎖は認識できる、という特性のB細胞とT細胞がそれぞれ無数の種類、作られてストックされていることになります
つまり兵隊さんは揃っていて、それぞれある1つのペプチドを認識できるわけですね。
これが平時の状態、としておきます。そうやって獲得免疫は体制を整えて待っているわけです
いざ病原体が入ってきたとき
さて、では病原体が身体に入った状況にもどります。
話を進めながら登場人物が増えます。
病原体が身体に入ってくると、すぐにペプチド認識がされて、攻撃が開始されるのかというと、そうではありません。そんなすぐに反応はしません。
まず、病原体をパクパク食べて消化するという役割の細胞が体にはいます。
そういう細胞は、パクパク食べて細胞のなかで病原体を消化したあと、その消化断片であるペプチド鎖を細胞表面に提示します。
ペプチド鎖は抗体に認識されたりT細胞表面のTCRに認識されますが、これを、抗原 antigen といいます。
そして、パクパク食べて抗原を細胞表面にだす細胞のことを、抗原提示細胞 (antigen presenting cell; APC) と呼びます。
さて、このAPCは色んな種類がありますが、特に働きが強いのは3種なのです。
樹状細胞、単球・マクロファージそしてB細胞です。
あれ、B細胞は抗体を…とB細胞は混乱するので置いておきます。単球というのはパワーアップするとマクロファージになる細胞なのでが、これはパクパク食べる能力、貪食能の強い細胞です。
しかし実は最も大事な役割をはたすのは樹状細胞 (dendritic cell; DC) というものです。
この樹状細胞だけがナイーブT細胞をエフェクターT細胞に活性化することができるのです。はぁ?
突然ナイーブとかエフェクターとか、出てきてしまいました。それはなんじゃろな?
先ほどまで延々と話した沢山準備しておいた多種類が存在するT細胞ですが、これらはまだ病原体のペプチドに出会ったことはないものとします。
これが、敵をしらずまだまだウブということで、ナイーブT細胞 (または immature T細胞)と呼ばれるものです。
このナイーブT細胞は、APCである樹状細胞の表面に提示されたペプチドが自分のTCRで認識されるものであった場合、樹状細胞に刺激されます。言い換えると、ナイーブT細胞は樹状細胞表面に出ているペプチドとくっついて、刺激されるということになります。
これが、認識、になりますよね。
刺激されたナイーブT細胞は、ここで初めて頑張るぞ、頑張って働くぞ、となり、活性化し、増殖します。数も増えますし、機能を発揮しようとしていろいろな遺伝子が発現したりします。こういう風に動き出した状態のT細胞をエフェクターT細胞と総称しています。
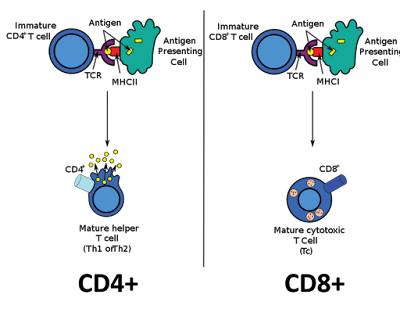
さて、上の図。エフェクターT細胞の分化する図、あれ、なんか2種類ありますね。ここでT細胞を見直す必要がでてきました。
免疫学が分からなくなる理由の1つは登場人物があまりに多いことにもあります。
とくに、一つの細胞内でいろんな種類があったりして…。
そう、T細胞は実は一枚岩ではなく、非常にたくさんの役割分担された亜集団からなっているのです。これが教科書では最初からこれでもかこれでもかと紹介されて混乱をまねくところなのです。
なので、混乱しないようにまずザックリT細胞を2つに分け、細かくは進みません。
その前に少し復習しますと、T細胞は、感染した細胞を壊すという細胞性免疫を担うのでした。しかし実は、先に述べたときはT細胞の「一部」、と書きました。伏線伏線。
実は、T細胞は細胞壊し屋さんだけでなく、司令塔となったり、B細胞などほかの種類の細胞を助けたりという役割をする亜集団もいるのです。
CD4とCD8
ここでT細胞をどうやってわけるか。形?形ではなかなかわかりません。
しかしいい方法があるのです。まずザックリ2つにわける方法として、明確なタンパク質の指標があるのです。それが細胞の表面に出ているCD4とCD8という分子なのです。
T細胞では、この CD4とCD8は、正常な細胞ではどちらかしか出ていません。発達の段階の途中では両方出てたりしますが、成長するとどちらか片方をほぼ必ずだしています。
そして、出ている分子がCD4なのかCD8なのかによって細胞の機能が大きく異なるのです。なんて便利なマーカーなんでしょう。
ここで、CD4を発現した、発現というのは、タンパク質が作られてでていることですが、発現したT細胞はなにをするかというと…他のT細胞を助ける、B細胞の分化成熟や抗体産生を助ける。ヘルプします。
よって、これをヘルパーT細胞と呼びます。くどいですが、ヘルパーT細胞はCD4陽性細胞です (陽性というのは検出できるという意味ですが、この場合には発現しているという意味ですね。逆は陰性になります)。
さて、逆のCD8陽性細胞はというと、これこそがウイルス感染細胞などを破壊する細胞で、キラーT細胞と呼ばれます。別名としては細胞傷害性T細胞 (cytotoxic T lymphocyte; CTL) とも言います。
登場人物が増えましたね。
リンパ球は主にB細胞とT細胞でした。
このうちT細胞はヘルパーT細胞と細胞障害性T細胞に別れました。
さぁ、まだわかれます…!分かれるんです。
このうちヘルパーT細胞、CD4陽性細胞は、分泌するサイトカインという分子の種類により、Th1細胞、Th2細胞、Th17細胞にわかれます。ぎゃー‼️めちゃくちゃや!
これ以上は…この時点ではメインストリームとは言いがたいので引き返しますが、Th1細胞は細胞性免疫をヘルプ、Th2細胞は液性免疫をヘルプ、Th17細胞は自己免疫の調整など、機能が違います。
大事なことは、ヘルプ機能があるということで、最も基本的なのはTh2です (図の中のTreg というのはまた改めて補足で話していくことになるかもしれません)。
さてここでTh2 は液性免疫、つまりB細胞を助けます。
B細胞にサイトカインなとよばれる連絡をするための分子をかけて活性化させるのです。
大分深入りしましたね、しかし流れを見直せば大丈夫です。見直しましょう。
病原体が来ると、抗原提示細胞が食べてペプチドを提示します。それを認識したナイーブT細胞が活性化してエフェクターT細胞になる。まずは、それだけですね。
ヘルプ機能
さて、エフェクターの片割れヘルパーT細胞のうちTh2はB細胞を助けます(今は、としておいてください、実際にはいまは Tfh とよばれるT細胞が行っていることがわかっています)。どう助けるのか。ここで、共刺激という考え方がでてきます。
共刺激とは、ある意味セーフティネットというかプルーフなのですが、免疫細胞はいくつかの刺激を共に同時に受けて初めて刺激がしっかり入る、というものです。
一つの刺激だけではすぐには刺激をうけず、暴走しないんですね
さて、B細胞。抗体を作るのでした。しかし実は抗体はミサイルのごとく打ち出すだけではなく、その抗体分子が細胞表面にも付いているのです。
これを特別にB細胞抗原受容体 (B cell receptor, BCR) と呼びます。打ち出す抗体と同じペプチドを認識します。
抗原提示細胞、実はT細胞だけに抗原提示をしているのではありません。
B細胞もBCRを使ってペプチドを認識しています。
そしてそれら、抗原提示はリンパ節など、リンパ組織とよばれる狭い限られたところで起こっているのですが、T細胞とB細胞は同じペプチドを近くで、抗原提示細胞によって提示されていることになります。
ここで共刺激の伏線を回収します。 実はB細胞の活性化には、B細胞受容体、B細胞補助受容体 (CD21などの分子なんです)、CD4陽性T細胞からのシグナルの3つが必要なのです。
補助受容体は抗原提示細胞から、刺激されます。
すなわち、病原体がパクパク食べられ、ペプチド提示がT細胞とB細胞にされる、それも近くで。
T細胞の一部はTh2となりB細胞にサイトカインという活性化分子を振りかける。B細胞は抗原提示されていて、共刺激で活性化します。
さてここで、活性化B細胞とは、すなわち抗体産生に特化した細胞であり、形質細胞 (plasma cell )と名前を変えます。そして抗体を打ち出して、ウイルス表面にべたべた付ける。この抗体は抗原提示されたペプチドと同じ配列ですから、病原体に特異的にくっつきますよね。
これで液性免疫は稼働しました。
この後、液性免疫は最適化していきますが、それは後に。
残りのT細胞をみます。残しておいたCD8陽性細胞。
細胞性免疫をつかさどるCTL
CD8陽性細胞は細胞障害性T細胞 (CTL)でした。
お仕事は、感染細胞をぶち壊します。どうやって壊すか。シンプルなんです。
感染細胞は細胞内に入ってきたウイルスなどの成分を分解して細胞表面に出します。説明を、省いていましたが、ペプチドはある、優勝カップというかお皿のようなものに乗っけられて表面に提示されます。
この、カップの名前が主要組織適合遺伝子複合体 (major histocompatibility complex; MHC) といい、ヒトにおいてはヒト白血球型抗原 (Human Leukocyte Antigen; HLA) です。
きいたことがあるかなぁ、白血球の血液型みたいなもので、拒絶反応などにも関係するんですね。
さて、またもどります。
感染細胞はこのMHCに、自分の細胞内で分解したウイルスのペプチドを乗せて提示します。するとCD8陽性のCTLはこれをTCRをつかって認識し、CD4陽性細胞のヘルプを得つつ、感染細胞を攻撃します。
CTLは細胞の膜に穴を開けるパーフォリン、細胞を分解するグランザイムなどをかけたり、細胞の自殺をうながす Fas 分子を刺激します。
こういう流れで、抗原提示後には液性免疫も細胞性免疫も、提示されたペプチド特異的に発動されるんですね。
さて、抗体の細かい作用は、またにしますが、これらが発動されると、病原体も感染細胞も、除去されます。これが第1段階の獲得免疫の機能のオーバービューなのですが、まだ、記憶、の話がされてませんね
免疫記憶をごく簡単に
免疫の記憶は実際には複雑ですが、概要は単純です。
すなわち、一度活性化したB細胞、ヘルパーT細胞、細胞障害性T細胞の一部は、メモリー細胞として身体に残って潜むんです。一度活性化すると性質が、少し変わります。抗体も最適化されます。そして待つ。
再び、同じペプチドが体内に取り込まれて抗原提示されたとき、メモリー細胞たちは速やかにエフェクター細胞として、活性化します。また、抗体はちょびちょび作られていて、ベースにすでに液性免疫が稼働しているんですね
というわけで、ざっくりと
これが獲得免疫のメインストリームの枝葉末節きりおとしの、オーバービューのエッセンスです。まずはメインストリームです。あとで追加したり、調整機構の修正、もっとたくさんの登場人物の紹介をしないといけません。
しかし一巡目はこれでいいかなと思います。ざっくりと獲得免疫の話をしました。
では次は
次は自然免疫を話して、その後、これらの免疫機構のオーバーラップと発達、詳細の補充と、疾患の実際、研究のフロンティアと進むのがいいのかなぁと思います。
繰り返しますが、何巡もする必要があります。また獲得免疫の話にも戻ってくるんですね。
ということで、第二回はこれでおしまい。また次に。